Zadanie 2.
Zadanie 2:
Opracowanie procedury badania immunologicznego (immunofenotypu) oraz przeciwciał przeciw heparynowych anty-PF4 dla określenia związku pomiędzy funkcją immunologiczną a produkcją przeciwciał ochronnych lub progresją zakażenia i jego powikłań zakrzepowych.
W ramach zadania zidentyfikowano biomarkery wyczerpania immunologicznego CD200 i PD1/PDL1 jako markery ciężkiego przebiegu zakażenia i ryzyka zgonu osób z COVID-19. Dla limfocytów T i B PD-1-dodatnich zaobserwowano znaczny wzrost ekspresji między grupą kontrolną a pacjentami z umiarkowanym lub ciężkim COVID-19 . Wszystkie markery związane z PD-1 i PD-L1 były stabilne w czasie dla analizowanych punktów czasowych w grupach z umiarkowanym i ciężkim COVID-19 co świadczy o ich wartości jako markerów prognostycznych w COVID-19.
Cząsteczka różnicowania CD200 jest glikoproteiną, której ekspresję rejestruje się na wielu komórkach układu odpornościowego, w tym na limfocytach T z receptorem CD4+ i CD8+ oraz limfocytach B z receptorem CD19+. CD200 jest ligandem CD200R, którego inhibicyjny wpływ na układ odpornościowy został potwierdzony w wielu stanach zapalnych, także wywołanych czynnikami zakaźnymi i nowotworowymi. W ramach badania immunofenotypu oraz obecności przeciwciał p-w heparynowych przeprowadzono analizy CD200 oraz oznaczono przeciwciała anty-PF4 u osób z rozpoznanym COVID-19. Badanie p-w ciał p-w heparynowych anty-PF4 przeprowadzono u 1876 osób, obserwując obecność IgM u 13.0% osób a IgG u 4.3% pacjentów. Nie obserwowano związku pomiędzy produkcją tych przeciwciał i progresją zakażenia lub powikłań przeciwzakrzepowych. Badania wykonywane są z wykorzystaniem cytometrii przepływowej w barwieniu dwukolorowym, tj. z przeciwciałem dedykowanym subpopulacji CD4, CD8, CD19 oraz CD200/CD200R
Dodatkowo analizowano charakterystykę przeżywalności , włączając ryzyko powikłań zatorowo-zakrzepowych u pacjentów leczonych Tocilizumabem.
Do tej analizy początkowo przeanalizowano 182 przypadki pacjentów z COVID-19 i zajęciem płuc >50% oraz biochemicznymi wskaźnikami burzy cytokinowej cytokin (Il-6 >100 pg/ml) przy zastosowaniu analiz przeżycia Kaplana-Meyera oraz wieloczynnikowych modeli Coxa. W badanej grupie pacjentów 100 (55%) było leczonych TCZ, a 82 (45%) nie otrzymało TCZ. Grupy były zrównoważone pod względem demografii, zajęcia płuc i markerów biochemicznych. Całkowita śmiertelność w grupie wyniosła 63,1%. Śmiertelność w grupie TCZ wyniosła 58,0% w porównaniu z 69,5% (n = 57) w grupie bez TCZ (p = 0,023). W wieloczynnikowych modelach proporcjonalnego ryzyka Coxa dożylne podanie tocilizumabu wiązało się z mniejszym prawdopodobieństwem przyjęcia na OIT (HR: 0333 (CI: 0,159–0,700, p = 0,004)) i niższą śmiertelnością (HR: 0,57306 (CI: 0,354–0,927, p = 0,023)), co pozwoliło na podsumowanie, że tocilizumab jest skuteczny w leczeniu najciężej chorych pacjentów z COVID-19 u których stopień zajęcia płuc procesem zapalnym może przekraczać 50% przy obecnej burzy cytokinowej z poziomem interleukiny 6 > 100 pg/ml.
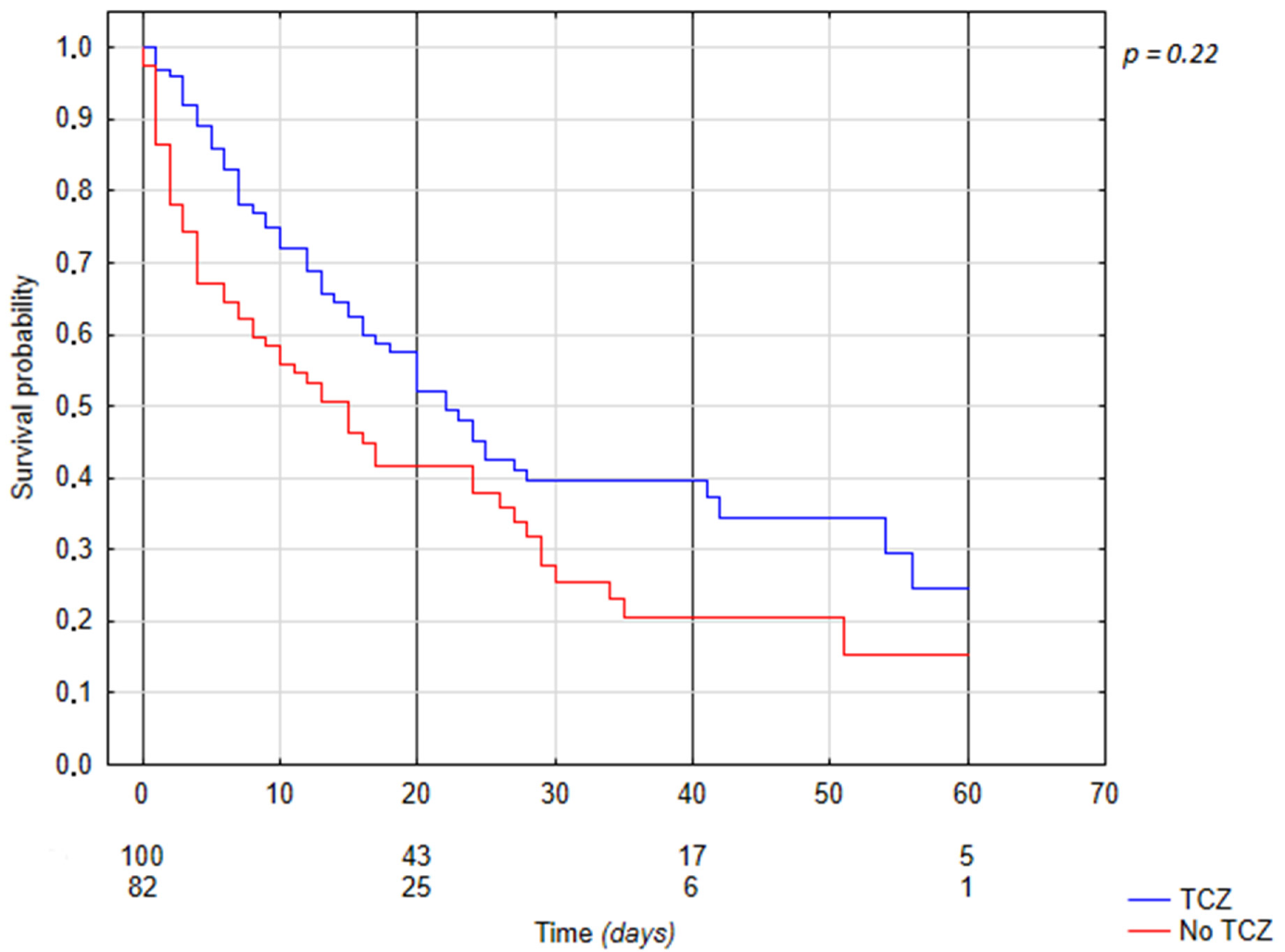
Rycina: Przeżycie osób z burzą cytokinową leczoną i nieleczoną Tocilizumabem (TCZ) – analiza jednoczynnikowa.
Częściowe wyniki zadania opublikowano w pracy:
Chober D, Aksak-Wąs B, Bobrek-Lesiakowska K, Budny-Finster A, Hołda E, Mieżyńska-Kurtycz J, Jamro G, Parczewski M. Effectiveness of Tocilizumab in Patients with Severe or Critical Lung Involvement in COVID-19: A Retrospective Study. J Clin Med. 2022 Apr 20;11(9):2286. doi: 10.3390/jcm11092286. PMID: 35566412; PMCID: PMC9101084




